
Aminotransferasen
| Aminotransferasen | ||
|---|---|---|
| ||
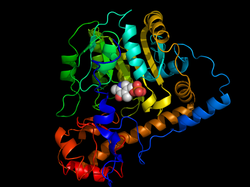
| Bändermodell der Aspartat-Transaminase nach
PDB
| ||
| Enzymklassifikation | ||
| EC, Kategorie |
| |
| Reaktionsart | Übertragung von Aminogruppen (Transaminierung) | |
Aminotransferasen oder Transaminasen sind Enzyme in allen Lebewesen, welche die Übertragung von α-Aminogruppen von einem Donor- auf ein Akzeptormolekül katalysieren (Transaminierung).
Eigenschaften
Bei einer medizinischen Laboruntersuchung auf Transaminasen handelt es sich um die Messung der Blutwerte für die Aspartat-Aminotransferase (ASAT) und die Alanin-Aminotransferase (ALAT), die diagnostische Bedeutung bei Lebererkrankungen haben (Transaminasenanstieg).
Transaminasen sind unentbehrlich im Aminosäurestoffwechsel und bei der Hexosamin-Biosynthese. Außerdem ist eine Glutamat-1-semialdehyd-Aminotransferase bei Bakterien und Archaeen an der Porphyrin-Biosynthese beteiligt. Transaminasen werden durch Transaminaseinhibitoren gehemmt.
Katalysierte Reaktion
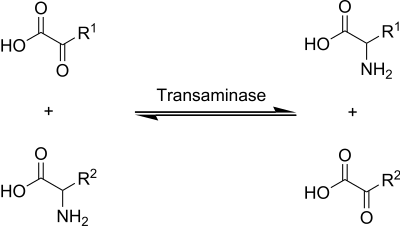
Üblicherweise handelt es sich bei dem Donor um eine Aminosäure und bei dem Akzeptor um eine α-Ketosäure, wobei aus der Aminosäure eine neue α-Ketosäure und aus der ursprünglichen α-Ketosäure eine neue Aminosäure wird. Als Cofaktor ist in vielen Fällen Pyridoxalphosphat beteiligt.
Transaminasen gibt es für 19 der 20 proteinogenen Aminosäuren, wodurch diese eigentlich nur bedingt essenziell sind. Sie können aus speziellen Ketosäuren konvertiert werden, von denen einige ihrerseits vom Stoffwechsel jedoch nicht bereitgestellt werden. Die Partneraminosäure ist dabei meist Glutamat, das zu α-Ketoglutarat desaminiert wird und so als universeller Spender für Aminogruppen dient. Daher wird Glutamat in der Benennung der Transaminase meist weggelassen.
Literatur
- Ulf Dettmer, Malte Folkerts, Eva Kächler, Andreas Sönnichsen: Intensivkurs Biochemie (Elsevier-Verlag, München, 1. Auflage 2005, ISBN 978-3437444500
- Smith DM, Thomas NR, Gani D: A comparison of pyridoxal 5'-phosphate dependent decarboxylase and transaminase enzymes at a molecular level.
In: Experientia. 47. Jahrgang, Nr. 11–12,
Dezember 1991, S. 1104–18,
 PMID 1765122.
PMID 1765122. - Rossi F, Schwarcz R, Rizzi M: Curiosity to kill the KAT (kynurenine aminotransferase): structural insights into brain kynurenic acid synthesis.
In: Curr. Opin. Struct. Biol. 18.
Jahrgang, Nr. 6, Dezember 2008,
S. 748–55,
 PMID 18950711.
PMID 18950711. - Yonaha K, Nishie M, Aibara S: The primary structure of omega-amino acid:pyruvate aminotransferase.
In: J. Biol. Chem. 267. Jahrgang, Nr. 18,
Juni 1992, S. 12506–10,
 PMID 1618757.
PMID 1618757.


© biancahoegel.de
Datum der letzten Änderung: Jena, den: 21.04. 2024