Drospirenon
| Sicherheitshinweise | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ||||||||||||||||
| Toxikologische Daten | 500–2000 mg/kg (LD50, Ratte, oral) | |||||||||||||||
Drospirenon ist ein synthetisch hergestellter Arzneistoff aus der Gruppe der Gestagene, der von Schering (heute Bayer HealthCare) entwickelt wurde und als wirksamer Bestandteil in „Antibabypillen“ wie beispielsweise Yasmin enthalten ist.
In seinen pharmakologischen Eigenschaften ist Drospirenon dem natürlich vorkommenden Hormon Progesteron sehr ähnlich und hat wie dieses antiandrogene und antimineralocorticoide Eigenschaften. Orale Kontrazeptiva („Antibabypillen“) mit Drospirenon als gestagene Komponente können durch die antiandrogene Wirkung zur Therapie bei unreiner Haut (Akne) eingesetzt werden und tragen dazu bei, das Hauterscheinungsbild zu verbessern. Durch die antimineralkortikoide Aktivität kann einer Gewichtszunahme und anderen Symptomen, die eine Folge von Flüssigkeitseinlagerung darstellen (z.B. Brustspannen) vorgebeugt werden. Kritik an diesem Wirkstoff besteht insbesondere in der Annahme eines erhöhten Thromboserisikos (s.u.), das im Zusammenhang mit der entwässernden und damit blutverdickenden Wirkung bei Einnahme von Drospirenon enthaltenden oralen Kontrazeptiva postuliert wurde.
Chemisch leitet sich Drospirenon vom Aldosteronantagonist Spironolacton ab.
| Strukturformel | |
|---|---|
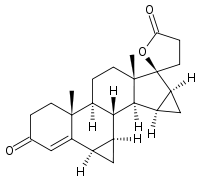 | |
| Allgemeines | |
| Freiname | Drospirenon |
| Andere Namen | 6β,7β;15β,16β-Dimethylen-3-oxo-17α-pregn-4-en-21,17-carbolacton |
| Summenformel | C24H30O3 |
| CAS-Nummer | 67392-87-4 |
| PubChem | 68873 |
| ATC-Code |
|
| DrugBank | DB01395 |
| Kurzbeschreibung | weißes bis fast weißes Pulver |
| Arzneistoffangaben | |
| Wirkstoffklasse | Gestagene |
| Eigenschaften | |
| Molare Masse | 366,49 g/mol |
| Schmelzpunkt | 201,3 °C |
| Löslichkeit | praktisch unlöslich in Wasser, leicht löslich in Dichlormethan, löslich in Aceton und Methanol, wenig löslich in Ethanol |
Geschichtliches
Wiechert und Mitarbeiter synthetisierten bereits 1976 Drospirenon bei der Schering AG. Allerdings dauerte es rund 25 Jahre, bis dessen pharmakologisches Potential erkannt und der Arzneistoff im Jahre 2000 auf den Markt gebracht wurde.
Thromboserisiko
Generell führen Ovulationshemmer („Antibabypillen“) zu einem ca. 3-6-fach erhöhten Thromboserisiko. Drospirenon steht im Verdacht eines (verglichen mit anderen Ovulationshemmern) erhöhten Thromboserisikos. Die Frage kann derzeit noch nicht als abschließend geklärt betrachtet werden.
In epidemiologischen Studien aus Holland und Dänemark vom August 2009 wurde erneut über ein erhöhtes Thromboserisiko im Zusammenhang mit dem Wirkstoff Drospirenon berichtet. Das Risiko stieg dabei mit zunehmendem Alter der Frau und höherem Östrogengehalt der Pille. Diese und andere Untersuchungen wurden von der Arzneimittelkommission der deutschen Ärzteschaft(AkdÄ) zum Anlass genommen, die aktuelle Einschätzung des Risikos von thromboembolischen Ereignissen unter hormonaler Kontrazeption darzustellen und Hinweise für die Verordnung zu geben. Zwei im Jahre 2010 veröffentlichte Untersuchungen kamen jedoch zu dem Schluss, dass Drospirenon in Antibabypillen das Risiko von venösen oder arteriellen Thrombosen nicht stärker erhöht als der Wirkstoff Levonorgestrel (älteres Gestagen der 2. Generation) und anderen älteren Gestagenen. Somit ist unklar, ob Drospirenon-haltige Antikonzeptiva das Thromboserisiko tatsächlich stärker erhöhen als Antikonzeptiva mit Gestagenen wie Desogestrel oder Gestoden. Im Februar 2013 leitete die europäische Arzneimittelagentur ein Risikoberwertungsverfahren für kombinierte orale Kontrazeptiva ein, die Drospirenon oder andere Progestagene der 3. und 4. Generation enthalten.
Wahrnehmung in den Medien
„Die Zeit“ berichtete 2010 von Klagen von Patientinnen, die durch Drospirenon Thrombosen und Embolien erlitten, gegen den pharmazeutischen Unternehmer Bayer HealthCare. Bis April 2010 waren lt. „Die Zeit“ 1750 Klagen gegen Bayer HealthCare in den USA bekannt, außerdem mehrere in Deutschland und der Schweiz. In Österreich wurde Drospirenon ebenfalls in den Medien diskutiert. Aktuell sind allein in den USA rund 7.000 Klagen gegen Bayer anhängig. Ende Mai 2011 reichte erstmals auch eine deutsche Geschädigte Klage gegen die Bayer AG ein. Im April 2012 berichtete Spiegel Online, dass Bayer insgesamt in einem Vergleich rund 142 Millionen US-Dollar (107 Millionen Euro) an 651 betroffene Frauen zahlen werde. Bis September 2012 hat sich die Entschädigungssumme in den USA auf 500 Millionen Euro erhöht. Mit Stand 2013 wurden in den USA von Bayer über 7600 Frauen mit der Summe von 1,575 Milliarden Dollar entschädigt, dies ohne Anrechnung einer Schuld.
Am 5. November 2015 eröffnet das Landgericht Waldshut-Tiengen einen Zivilprozess gegen Bayer. Die Studentin Felicitas Rohrer aus Bad Säckingen verlangt von dem Unternehmen Schadenersatz und Schmerzensgeld in Höhe von 200.000 Euro wegen Gesundheitsschäden, die durch Yasminelle entstanden sein sollen. Der Anwalt von Klägerin Rohrer vertritt noch acht weitere Frauen, die sich durch Bayer-Verhütungspillen geschädigt sehen.
Herstellung
Die vielstufige hochkomplexe Synthese geht von 5-Androsten-3β-ol-17-onacetat aus.
Handelsnamen
- Kombination mit Ethinylestradiol: aida (D), Aliane (A), Petibelle (D), Yasmin (D, A, CH, US), Yasminelle (D, A, CH), YAZ (D, A, CH, US), Yirala (A), sowie Generika (D, A, CH)
- Kombination mit Estradiol: Angeliq (D, A, CH, US)


© biancahoegel.de
Datum der letzten Änderung: Jena, den: 10.05. 2023