
Phosphoglyceratmutase
| Phosphoglyceratmutase | ||
|---|---|---|
| ||
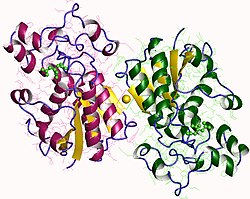
| Phosphoglyceratmutase 1 (B type) dimer (Mensch) nach
PDB | ||
| Eigenschaften des menschlichen Proteins | ||
| Masse/Länge Primärstruktur | 253/252/254/270 Aminosäuren | |
| Sekundär- bis Quartärstruktur | Homodimer | |
| Bezeichner | ||
| Gen-Namen | | |
| Enzymklassifikationen | ||
| EC, Kategorie | | |
| Reaktionsart | Umlagerung | |
| Substrat | 2-Phosphoglycerat | |
| Produkte | 3-Phosphoglycerat
5.4.2.12 | |
| Vorkommen | ||
| Übergeordnetes Taxon | Lebewesen | |
Phosphoglyceratmutasen (PGM oder PGAM) sind Enzyme, die die Umlagerung der Phosphatgruppe in Phosphoglycerat von 2- auf 3-Position und umgekehrt katalysieren. Diese Reaktion ist ein Teilschritt in der Glycolyse, der Verwertung von Kohlenhydraten im Stoffwechsel aller Lebewesen, die in jeder Zelle stattfindet. Es wird zwischen Cofaktor-abhängigen (dPGM, EC
![]() 5.4.2.11) und Cofaktor-unabhängigen (iPGM, EC
5.4.2.11) und Cofaktor-unabhängigen (iPGM, EC
![]() 5.4.2.12) Enzymen unterschieden. Erstere benötigen
2,3-Diphosphoglycerat als Kofaktor und finden sich in allen Wirbeltieren, einigen Wirbellosen, Pilzen und Bakterien.
Zweitere sind in allen Pflanzen und Algen sowie einigen Wirbellosen, Pilzen
und Bakterien verbreitet.[1] Mit den Säugetieren haben sich durch Kopie zusätzliche
Allele des PGAM1-Gens gebildet, die PGAM2, PGAM4 und PGAM5 genannt werden. PGAM2 wird nur in den Muskeln produziert.
Mutationen am PGAM2-Gen führen zu einer Form der Muskeldystrophie.
5.4.2.12) Enzymen unterschieden. Erstere benötigen
2,3-Diphosphoglycerat als Kofaktor und finden sich in allen Wirbeltieren, einigen Wirbellosen, Pilzen und Bakterien.
Zweitere sind in allen Pflanzen und Algen sowie einigen Wirbellosen, Pilzen
und Bakterien verbreitet.[1] Mit den Säugetieren haben sich durch Kopie zusätzliche
Allele des PGAM1-Gens gebildet, die PGAM2, PGAM4 und PGAM5 genannt werden. PGAM2 wird nur in den Muskeln produziert.
Mutationen am PGAM2-Gen führen zu einer Form der Muskeldystrophie.
Katalysierte Reaktion
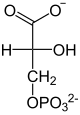 ⇔
⇔ 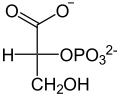
2-Phosphoglycerat wird umgelagert zu 3-Phosphoglycerat und umgekehrt. Bei der Cofaktor-abhängigen Form erfolgt die Katalyse durch zwischenzeitliche Bildung eines Phosphohistidin-Restes in der PGAM. Dabei ist zu beachten, dass ein zusätzlicher Phosphatrest an C2 angelagert wird und somit das Zwischenprodukt 2,3-BPG entsteht.
Erst danach wird der Phosphatrest an C3 entfernt und die Mutase erhält die Phosphorylgruppe zurück, um den Phosphohistidin-Rest zu regenerieren.
Das Enzym benötigt katalytische Mengen an 2,3-Bisphosphoglycerat, um den Histidinrest im aktiven Zentrum in phosphorylierter Form zu halten.[2]
Weitere Funktionen
Die PGAM-Isoformen haben zusätzlich schwache Aktivität als Bisphosphoglyceratmutase (EC
![]() 5.4.2.4) und als Biphosphoglycerat-Phosphatase (EC
5.4.2.4) und als Biphosphoglycerat-Phosphatase (EC
![]() 3.1.3.13).
3.1.3.13).
PGAM1 wird in Krebszellen im Übermaß produziert. PGAM1 bindet in vitro am Kern von Hepatitis-C-Virus. Patienten mit autoimmuner Hepatitis erzeugen vermehrt PGAM1-Antikörper.[3][4][5]
PGAM5 wird an die Außenmembran von Mitochondrien transportiert und bindet dort Keap1 und Nrf2.[6]
Einzelnachweise
- ↑ Mark J Jedrzejas: Structure, function, and evolution of phosphoglycerate mutases: comparison with fructose-2,6-bisphosphatase, acid phosphatase,
and alkaline phosphatase. In: Progress in Biophysics and Molecular Biology. Band 73,
Nr. 2–4, Februar 2000, S. 263–287,
doi:
 10.1016/S0079-6107(00)00007-9
(
10.1016/S0079-6107(00)00007-9
(  elsevier.com [abgerufen am 5. August 2025]).
elsevier.com [abgerufen am 5. August 2025]).
- ↑ Jeremy M. Berg, John L. Tymoczko, Lubert Stryer, Gregory J. Gatto jr.: Stryer Biochemie. Springer-Verlag, 2014,
ISBN 978-3-8274-2988-9, S. 467
(
 eingeschränkte Vorschau in der Google-Buchsuche).
eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ F. Lu et al.: Serum proteomic-based analysis for the identification of a potential serological marker for autoimmune hepatitis. Biochem Biophys Res Commun.
367/2/2008:284-90.
 PMID 18154727
PMID 18154727
- ↑ H. X. Su et al.: Screening cellular proteins binding to the core region of hepatitis C virus RNA genome with digoxin-labeled nucleic acids. Intervirology.
50/4/2007:303-9.
 PMID 17622790
PMID 17622790
- ↑ L. J. Huang et al.: Proteomic analysis of secreted proteins of non-small cell lung cancer. Ai Zheng. 25/11/2006:1361-7.
 PMID 17094902
PMID 17094902
- ↑ S. C. Lo und M. Hannink: PGAM5 tethers a ternary complex containing Keap1 and Nrf2 to mitochondria. Exp Cell Res. 314/8/2008:1789-803.
 PMID 18387606
PMID 18387606


© biancahoegel.de
Datum der letzten Änderung: Jena, den: 17.09. 2025