Glycerin
| Sicherheitshinweise | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| |||||||||
| MAK | 50 mg/m3 | ||||||||
| Toxikologische Daten | 4090 mg/kg (LD50, Maus, oral) | ||||||||
Glycerin (von gr. glykerós ‚süß‘ , nach IUPAC Glycerol, auch Glyzerin) ist der Trivialname und die gebräuchliche Bezeichnung von Propan-1,2,3-triol. Glycerin ist ein Zuckeralkohol und der einfachste dreiwertige Alkohol, ein Triol. Der Name Glycerol wurde eingeführt, da er die korrekte Endung -ol für einen Alkohol besitzt (die Endung -in steht für Alkine oder Amine).
Glycerin ist in allen natürlichen Fetten und fetten Ölen als Fettsäureester (Triglyceride) vorhanden und spielt eine zentrale Rolle als Zwischenprodukt in verschiedenen Stoffwechselprozessen. Als Lebensmittelzusatzstoff trägt es das Kürzel E 422.
Geschichte
1779 erhielt Carl Wilhelm Scheele bei der Verseifung von Olivenöl erstmals Glycerin. Michel-Eugène Chevreul konnte im Jahr 1813 nachweisen, dass Fette Ester von Fettsäuren und Glycerin sind und gab dem Alkohol 1823 seinen Namen, abgeleitet von griechisch glykys, ‚süß‘.
| Strukturformel | |
|---|---|
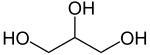 | |
| Allgemeines | |
| Name | Glycerin |
| Andere Namen |
|
| Summenformel | C3H8O3 |
| CAS-Nummer | 56-81-5 |
| PubChem | 753 |
| ATC-Code |
|
| DrugBank | DB04077 |
| Kurzbeschreibung | farblose, schwerbewegliche Flüssigkeit |
| Eigenschaften | |
| Molare Masse | 92,09 g/mol |
| Aggregatzustand | flüssig |
| Dichte | 1,26 g/cm3 (20 °C) |
| Schmelzpunkt | 18 °C |
| Siedepunkt | 290 °C (unter Zersetzung) |
| Dampfdruck | < 0,1 Pa (20 °C) |
| Löslichkeit |
|
| Brechungsindex | 1,4745 |
| Thermodynamische Eigenschaften | |
| ΔHf0 | −669,6 kJ/mol |
Gewinnung und Darstellung
Die Herstellung kann petrochemisch aus Propen mit den Zwischenprodukten Allylchlorid und Epichlorhydrin oder chemisch als Nebenprodukt bei der Verseifung von natürlichen Fetten und Ölen zur Gewinnung von Seifen (= Alkalisalze der Fettsäuren) geschehen. Früher wurden dazu vor allem tierische Fette eingesetzt.
Inzwischen werden große Mengen Glycerin als Nebenprodukt der Biodieselherstellung erzeugt. Dies geschieht durch eine Umesterung von meist pflanzlichen Ölen mit Methanol. Ein Fettmolekül (Triacylglycerid) wird mit drei Methanolmolekülen zu Glycerin und drei Fettsäuremethylestern (FAME) umgesetzt.
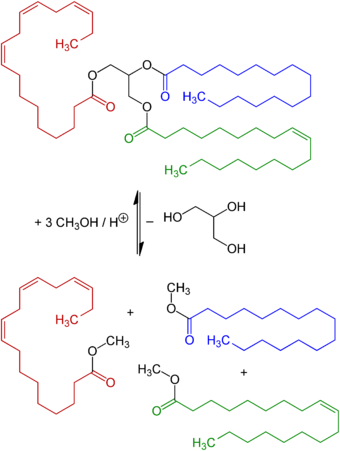
Auch eine biotechnologische Herstellung durch Fermentation ist möglich. Hefen können durch Sulfitzusatz die Gärung von Ethanolbildung auf Glycerinbildung umstellen. Als Substrat wurde oftmals Melasse verwendet, da diese neben einem hohen Anteil an Zucker auch viel Sulfit enthält. Diese Form der Gärung wurde 1918 von Carl Neuberg als 2. Neuberg'sche Gärungsform bezeichnet.
Glycerin ist in unterschiedlichen Reinheiten im Handel erhältlich. Für industrielle Zwecke wird es als Rohglycerin und für pharmazeutische Zwecke (Pharmaglycerin) in den Qualitäten 99,8-, 99,5- und etwa 86-prozentig angeboten. 86-prozentig (mit 14 % Wasser) ist es wegen des stark erniedrigten Schmelzpunkts (–10°C) und der niedrigeren Viskosität(ca. 100 mPa·s) technisch einfacher zu handhaben. Die Aufbereitung erfolgt durch mehrstufige Destillation, Desodorierung und Filtration. Hochreines, synthetisches Glycerin stammt nicht aus tierischen oder pflanzlichen Vorprodukten und wird besonders in qualitätssensiblen Bereichen der Pharmaindustrie sowie der Kosmetik- und Lebensmittelindustrie eingesetzt.
Eigenschaften
Physikalische Eigenschaften
Glycerin ist bei Raumtemperatur eine farb- und geruchlose, viskose und hygroskopische Flüssigkeit, die süßlich schmeckt. Glycerin hat eine Viskosität von 1480 mPa·s (20 °C).
Chemische Eigenschaften
Glycerin bildet unter Hitzeeinwirkung weißen Dampf. Beim Erhitzen unter Sauerstoffmangel zersetzt es sich, zu dem in Wasser gut (267 g/l) löslichen, sowie giftigen ungesättigten Aldehyd Propenal, das auch Acrylaldehyd oder Acrolein genannt wird.
Mit festem Kaliumperoxid reagiert es unter Selbstentzündung vollständig zu Kohlendioxid und Wasser.
Von wässrigem Kaliumperoxid wird es nur bis zur Mesoxalsäure oxidiert. (CSB-Titration durch Manganometrie)
Verwendung
Lebensmittel & Kosmetik
Wegen seiner wasserbindenden Eigenschaften ist Glycerin in Kosmetikartikeln als Feuchtigkeitsspender enthalten. Als Lebensmittelzusatzstoff findet Glycerin unter der Nummer E 422 Anwendung zur Feuchthaltung, etwa für Datteln oder Kaugummi, aber auch als Süßungsmittel.
Haushalt
Häufig wird Glycerin in das Wasser von Weihnachtsbaumständern gegeben, um den Baum länger frisch zu halten. Das Glycerin sorgt für Frostschutz und führt dazu, dass die Nadeln länger halten. Glycerin findet aufgrund seiner feuchtigkeitsspendenden Wirkung Verwendung in Lederpflegemitteln und Schuhcremes um Leder glatt und geschmeidig zu halten.
Tabak & Zigaretten
Glycerin (E 422) wird zusammen mit 1,2-Propandiol als Feuchthaltemittel für Tabakwaren verwendet, nicht zu verwechseln mit der Glycerin-Phosphorsäure und deren Natrium-, Kalium- und Magnesiumverbindungen deren Reinheitsanforderungen in der Tabakverordnung klar definiert ist. Im Zigaretten- und Pfeifentabak sollen die Feuchthaltemittel vor allem die Lagerungszeiten der Produkte verlängern und die Austrocknung verhindern. Shisha-Tabak werden von den Verbrauchern deutlich höhere Mengen an Feuchthaltemitteln zugemischt, um einerseits die Verbrennung des Tabaks zu verhindern und andererseits einen dichteren Rauch zu erzeugen. Weiterhin findet Glycerin ebenso wie 1,2-Propandiol Verwendung als Nebelfluid in elektrischen Zigaretten.
Industrie & Technik
Glycerin wird als Frostschutzmittel (in Mischung mit Wasser als Wärmeträger), Schmierstoff und Weichmacher verwendet. In Nebelfluiden wird es zur Erhöhung der Standzeit des Nebels beigesetzt. Bei der Herstellung von Kunststoffen, Microchips, Farbstoffen sowie Zahnpasta wird die Substanz als Reaktant benötigt. Bei der Reaktion mit einem Gemisch konzentrierter Salpetersäure und konzentrierter Schwefelsäure entsteht „Glyceroltrinitrat“. Diese Verbindung ist der als „Nitroglycerin“ bekannte Explosivstoff, der zusammen mit Kieselgur den SprengstoffDynamit bildet.
Aufgrund der zeitweise deutlich gesunkenen Preise werden neue Anwendungsgebiete für Glycerin gesucht. Neben der Verbrennung zur Energieerzeugung sind dabei insbesondere die Nutzung als zusätzliches Nährmedium (Cosubstrat) in Biogasanlagen zur Erzeugung von Biogas sowie die Nutzung als Fermentationssubstrat in der Industriellen Biotechnologie Alternativen.
Weiterhin wird geforscht, Glycerin mit Isobuten zu Glycerin-tert-Butylether (GTBE; analog zu MTBE und ETBE) umzusetzen für den Einsatz als Kraftstoffzusatz. Seit 2009 setzt die Volkswagen AG aus alten Frittierfetten gewonnenes Glycerin anstelle von aus Erdöl gewonnenem Ethylenglycol als Kühlmittelzusatz (G13) in ihren Fahrzeugmodellen ein.
Glycerin lässt sich in einem neuen Verfahren unter Einwirkung von Ameisensäurezu einem chemischen Grundbaustein – dem Allylalkohol – umsetzen.
Landwirtschaft
Bei wachsenden Futtermittelpreisen findet Glycerin als Futtermittel für Wiederkäuer, Schweine und Hühner Interesse.
Medizin
Glycerin wird in der Medizin als Arzneistoff zur Behandlung des Hirnödems eingesetzt. Dazu wird es als 10 %ige Lösung infundiert. In Form glycerinhaltiger Zäpfchen kommt es als Abführmittel (Laxans) zur Anwendung. Die Wirkung entsteht zum einen durch einen reflektorischen Effekt: Durch den Kontakt des Glycerins mit der Rektalschleimhaut wird der Defäkationsreiz gesteigert. Zum anderen wirkt ein osmotischer Effekt: Durch den Wassereinstrom in das Darmlumen wird der Stuhl weicher und gleitfähiger. Gegenstand medizinischer Forschung ist die Verwendung von Glycerin zur Aufrechterhaltung der menschlichen Hirn- und Organfunktionen während einer künstlichen Absenkung der Körpertemperatur. Dies könnte für langwierige schwierige medizinische Operationen von Bedeutung sein. Biologisches Vorbild ist der kanadische graue Laubfrosch Hyla versicolor, dessen Körperzellen sich zur Überwinterung mit Glycerin anreichern.
Biologische Bedeutung
Die meisten tierischen und pflanzlichen Fette und Öle sind Triacylglyceride (Triglyceride). Sie bestehen aus dem dreiwertigen Alkohol Glycerin, der über die Hydroxygruppen(–OH) dreifach mit Fettsäuren verestert ist. Sie sind Energiespeicher im Fettgewebe oder in Samen von Ölpflanzen, wie Raps, Soja und Sonnenblume. Ähnlich aufgebaut sind Phosphoglyceride. Statt der dritten Fettsäure ist eine Phosphatgruppe verestert und an diese ein Rest gekoppelt, wie Cholin im Lecithin. Somit erhält das Molekül einen polaren und einen apolaren Bereich, was die Bildung einer Membran (Zellmembran) ermöglicht.
Nahezu alle natürlich vorkommenden Glycerinderivate weisen die sn-Konfiguration auf, welche die räumliche Anordnung der Substituenten am mittleren Kohlenstoffatom des Glycerins festlegt.
Gesundheitsrisiken
Glycerin wird neben anderen Feuchthaltemitteln Wasserpfeifentabaken in erheblichen Mengen zugesetzt. Eine Untersuchung des Bundesinstitut für Risikobewertung (BfR) quantifizierte den Feuchthaltemittelgehalt im Wasserpfeifenrauch und konnte erhebliche Mengen der Feuchthaltemittel Glycerin und Propandiol (Propylenglycol) nachweisen. In der Bewertung der Ergebnisse wurde auf mögliche Gesundheitsgefahren hingewiesen, beispielsweise wurden im Tierversuch Veränderungen des Zellepithels im Kehlkopf und Reizungen der Nasenschleimhäute bis hin zum Nasenbluten festgestellt.


© biancahoegel.de
Datum der letzten Änderung: Jena, den: 11.03. 2024