
Eisen(II)-hydroxid
| Sicherheitshinweise | |||
|---|---|---|---|
|
Eisen(II)-hydroxid ist eine anorganische chemische Verbindung des Eisens aus der Gruppe der Hydroxide.
| Kristallstruktur | |
|---|---|
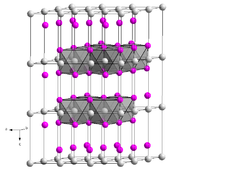
| |
| _ Fe2+ _ OH− | |
| Allgemeines | |
| Name | Eisen(II)-hydroxid |
| Andere Namen |
|
| Verhältnisformel | Fe(OH)2 |
| Kurzbeschreibung | weißer Feststoff |
| Externe Identifikatoren/Datenbanken | |
| CAS-Nummer | 18624-44-7 |
| EG-Nummer | 242-456-5 |
| ECHA-InfoCard | 100.038.581 |
| PubChem | 10129897 |
| Eigenschaften | |
| Molare Masse | 89,86 g/mol |
| Aggregatzustand | fest |
| Dichte | 3,4 g/cm3 |
| Löslichkeit |
|
Gewinnung und Darstellung
Eisen(II)-hydroxid erhält man durch Fällung aus Eisen(II)-Salzlösungen unter Sauerstoffausschluss (z.B. Ammoniumeisen(II)-sulfatlösung mit Natronlauge). Der weiße flockige Niederschlag verfärbt sich aber schnell dunkel unter Bildung von rotbraunem Eisen(III)-hydroxid.
Es bildet sich auch als Zwischenprodukt beim Rosten von Eisen, wobei es infolge des Luftsauerstoffs über wasserhaltiges Eisen(III)-hydroxid FeO(OH) weiter zu rotbraunem Eisen(III)-oxid bzw. bei Sauerstoffmangel zu grünem Magnetit-Hydrat und schwarzem Magnetit umgesetzt wird.
Eigenschaften
Eisen(II)-hydroxid ist ein nahezu weißer, an Luft unbeständiger Feststoff mit geringem, grünlichem Anflug. Er verbrennt beim Ausstreuen in die Luft unter Funkensprühen. Bei Ausschluss von Sauerstoff sind reine, insbesondere Nickel-, Kupfer- und Cobaltfreie Präparate in Berührung mit Kaliumchlorid-Lösung unterhalb 100 °C völlig stabil. Die Verbindung besitzt eine Kristallstruktur vom Cadmium(II)-hydroxid-Typ mit der Raumgruppe P3m1 (Raumgruppen-Nr. 164) (Gitterparameter a = 325,8 pm, c = 460,5 pm). Eisen(II)-hydroxid ist amphoter und löst sich in konzentrierten Laugen unter Bildung von blaugrünen Hydroxoferraten(II), z.B. Na4[Fe(OH)6].


© biancahoegel.de
Datum der letzten Änderung: Jena, den: 01.02. 2023