
Alanin
| Sicherheitshinweise | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| |||||||||
Alanin, abgekürzt Ala oder A, ist eine nicht-essentielle α-Aminosäure. Sie ist chiral, tritt also in zwei spiegelbildlichen Formen auf, wobei das L-Alanin eine proteinogene Aminosäure ist, die nach IUPAC auch als (S)-2-Aminopropansäure oder als (S)-Alanin bezeichnet wird. D-Alanin [Synonym: (R)-Alanin] findet man als Baustein des Mureins, der Grundsubstanz von Bakterienzellwänden. Daneben gibt es noch das nichtproteinogene β-Alanin.
Wenn in diesem Text oder in der wissenschaftlichen Literatur „Alanin“ ohne weiteren Namenszusatz (Präfix) erwähnt wird, ist L-Alanin gemeint.
Geschichte
| Strukturformel | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
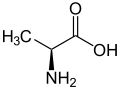 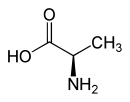
| ||||||||||||
| L-Alanin (links) bzw. D-Alanin (rechts) | ||||||||||||
| Allgemeines | ||||||||||||
| Name | Alanin | |||||||||||
| Andere Namen |
| |||||||||||
| Summenformel | C3H7NO2 | |||||||||||
| Kurzbeschreibung | farbloser bis gelblicher Feststoff | |||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||
| ||||||||||||
| Arzneistoffangaben | ||||||||||||
| ATC-Code | V06 | |||||||||||
| Eigenschaften | ||||||||||||
| Molare Masse | 89,10 g/mol | |||||||||||
| Aggregatzustand | fest | |||||||||||
| Dichte | 1,42 g/cm3 | |||||||||||
| Schmelzpunkt | 295–297 °C (Zersetzung) | |||||||||||
| pKs-Wert |
| |||||||||||
| Löslichkeit |
| |||||||||||

Neben Prolin gehört Alanin zu den beiden Aminosäuren, die erstmals durch Synthese dargestellt und nicht zuvor aus pflanzlichem oder tierischem Material isoliert worden sind. Alanin wurde 1850 von Adolph Strecker gefunden, als er eigentlich Milchsäure durch die Umsetzung von Acetaldehyd mit Ammoniak und Blausäure in Gegenwart von Salzsäure synthetisieren wollte, über die nach ihm benannte Strecker-Synthese. Strecker wählte dabei den Namen als Ableitung des Begriffs Aldehyd, da er die Aminosäure aus genanntem Acetaldehyd erhielt. Aus organischem Material wurde Alanin erstmals 1875 durch Paul Schützenberger erhalten, als dieser in einem Autoklaven mittels Baryt Seide aufspaltete und eine Mischung aus Glycin und Alanin identifizieren konnte. Von den am Aufbau der Proteinkette beteiligten Aminosäuren stellt L-Alanin 29,7 %.
Synthese
Die industrielle Herstellung von L-Alanin erfolgt ausgehend von der L-Asparaginsäure durch Abspaltung der β-Carboxygruppe in einem biotechnologischen Verfahren. Durch Strecker-Synthese gewonnenes racemisches Alanin kann an der Aminogruppe acetyliert werden und wird dann einer Racematspaltung unterworfen. Dabei wird unter Verwendung von L-Aminoacylase enantioselektiv die Acetylgruppe von L-N-Acetylalanin abgespalten und es entsteht L-Alanin, während D-N-Acetylalanin nicht hydrolysiert wird. Die Trennung von L-Alanin und D-N-Acetylalanin ist einfach. Benötigt man D-Alanin, so wird D-N-Acetylalanin unter sauren Bedingungen hydrolysiert, d.h., die Acetylgruppe wird abgespalten. Wenn kein Bedarf für D-Alanin besteht, wird das bei der kinetischen Racematspaltung anfallende D-N-Acetylalanin durch Einwirkung von Essigsäureanhydrid racemisiert und recycliert.
DL-Alanin kann auch aus 2-Brompropansäure synthetisiert werden, dieses Verfahren besitzt jedoch keine industrielle Bedeutung.
Im Stoffwechsel wird L-Alanin durch Transaminierung aus dem Endprodukt der Glykolyse, dem Pyruvat, synthetisiert. Bakterien erhalten benötigtes D-Alanin aus L-Alanin mittels des Enzyms Alaninracemase (EC 5.1.1.1).
Eigenschaften
Alanin liegt meist als „inneres Salz“ bzw. Zwitterion vor, dessen Bildung dadurch zu erklären ist, dass das Proton der Carboxygruppe an das freie Elektronenpaar des Stickstoffatoms der Aminogruppe wandert:
-
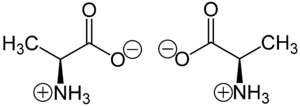
- Zwitterionen von L-Alanin (links) bzw. D-Alanin (rechts)
Beim physiologischen pH-Wert von 7,4 liegt ein großer Teil der Alanin-Moleküle als Zwitterion vor. Der isoelektrische Punkt von Alanin liegt bei pH 6,1 und Alanin erreicht seine geringste Löslichkeit in Wasser, da fast alle Alanin-Moleküle als Zwitterionen vorliegen. Die Lösung hat an diesem Punkt die geringste elektrische Leitfähigkeit, da Zwitterionen als Ganzes ungeladen sind.
Physiologische Funktionen
In Umkehrung dieser Synthese-Reaktion kann es enzymatisch auch wieder zu Pyruvat abgebaut werden (Transaminierung). So kann das Kohlenstoffgrundgerüst über Pyruvat wieder zum Aufbau von Glukose (Glukoneogenese) verwendet oder über den Zitronensäurezyklus vollständig zur Energiegewinnung abgebaut werden. Die oxidative Desaminierung des L-Alanins zu Pyruvat und Ammoniak, katalysiert durch das Enzym Alanin-Dehydrogenase, stellt eine weitere Abbaumöglichkeit dar; sie macht beispielhaft deutlich, wie ein Teil des Aminosäurestoffwechsels mit dem Kohlenhydratstoffwechsel verknüpft ist.
L-Alanin ist eine für den Menschen nicht-essentielle Aminosäure, kann also biosynthetisch durch den menschlichen Stoffwechsel hergestellt werden.
Alanin tritt – neben anderen Aminosäuren wie z.B. Leucin und Glutaminsäure – in α-Helices von Proteinen bevorzugt auf. Diese Aminosäuren begünstigen die Bildung dieses Sekundärstrukturelements und werden deshalb auch als Helixbildner bezeichnet.
Verwendung
Bestandteil von Infusionslösungen zur parenteralen Ernährung und von Diätetika.
Edukt in chemischen Synthesen
Die beiden Enantiomeren des Alanins werden, mit einer Schutzgruppe versehen, häufig für die Synthese von Peptiden und Proteinen eingesetzt. Weiterhin werden L- oder D-Alanin auch in der stereoselektiven Synthese als Edukt eingesetzt.
Siehe auch


© biancahoegel.de
Datum der letzten Änderung: Jena, den: 24.09. 2024